焦向英教授課題組發(fā)現TXNIP可通過PI3K/AKT信號通路參與胰島β細胞的增殖調控
糖尿病是一種由遺傳和環(huán)境等因素共同引起的,以胰島素絕對或相對缺乏為主要特征的慢性代謝性疾病�。胰島素是由胰島β細胞分泌產生的。因此����,胰島β細胞的數量減少和功能障礙是糖尿病發(fā)生發(fā)展的主要原因。目前治療糖尿病的主要手段是依靠控制飲食���,增加運動�����,使用降糖藥物,以達到控制血糖水平的目的�,但這些手段往往只能不同程度緩解糖尿病癥狀��,不能達到長期控制血糖或逆轉糖尿病進程的目的���,大多最終需要依賴胰島素。因此�����,促進胰島β細胞增殖����,恢復胰島β細胞數量及功能是治療糖尿病的最有效辦法。然而��,β細胞增殖的準確機制是什么�����?如何促進其增殖仍然不清楚�����。
山西醫(yī)科大學焦向英教授課題組長期從事硫氧還蛋白相互作用蛋白(Thioredoxin interacting protein���,TXNIP)的研究�。TXNIP是一種在多個組織器官中廣泛表達的多功能蛋白質。TXNIP的表達與糖尿病�����、心血管疾病�����、中樞神經系統(tǒng)疾病����、癌癥等多種疾病的發(fā)生發(fā)展密切相關,具有介導氧化應激�、誘導細胞凋亡及抑制細胞增殖等作用。
TXNIP是一種重要的腫瘤抑制因子�����,參與細胞生長調控�����,具有抑制細胞增殖和阻滯細胞周期進程的作用���。但TXNIP是否也參與胰島β細胞的增殖調控�����,目前也無報道�,有待觀察�����。
課題組構建了TXNIP基因敲除小鼠模型�����。正常生理條件下�����,成年胰島β細胞增殖能力低下�����,基本不發(fā)生增殖��。因此���,該課題組采用高脂喂養(yǎng)誘導胰島β細胞的代償性增殖模型�����,觀察TXNIP對胰島β細胞增殖的作用并進一步闡明其作用機制���。
TXNIP基因敲除小鼠血糖水平降低���,血清胰島素水平升高。進一步研究發(fā)現TXNIP基因敲除可以增加高脂喂養(yǎng)的肥胖小鼠胰島β細胞質量(β cell mass)(圖1)���。
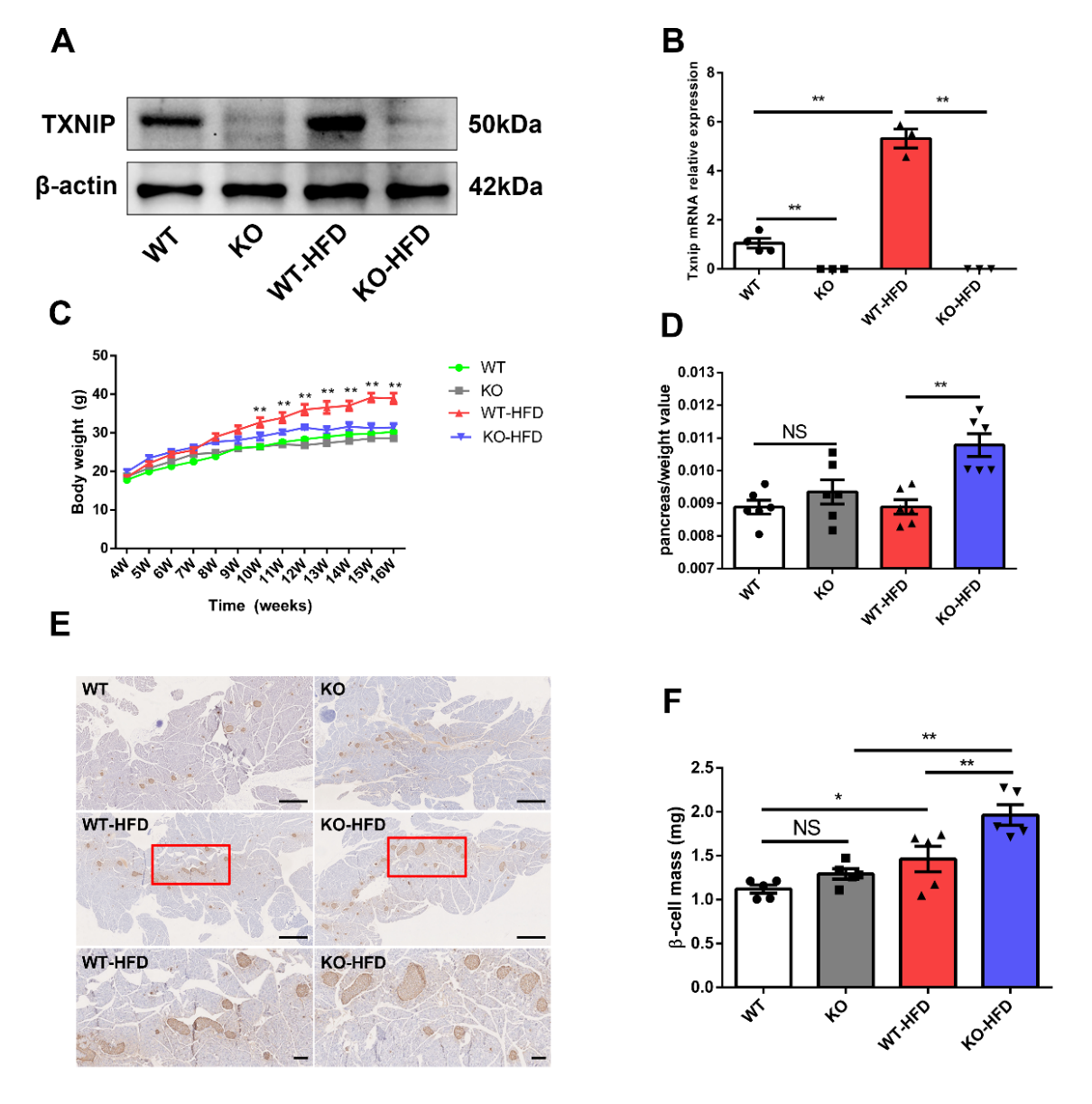
圖1
隨后課題組分別進行了Ki67和PCNA的免疫熒光染色�。結果顯示��,TNXIP基因敲除的高脂喂養(yǎng)小鼠胰島中Ki67和PCNA陽性細胞數量顯著增多(圖2)��。提示TNXIP基因敲除可以促進高脂喂養(yǎng)誘導的肥胖模型小鼠中胰島β細胞的代償性增殖��。
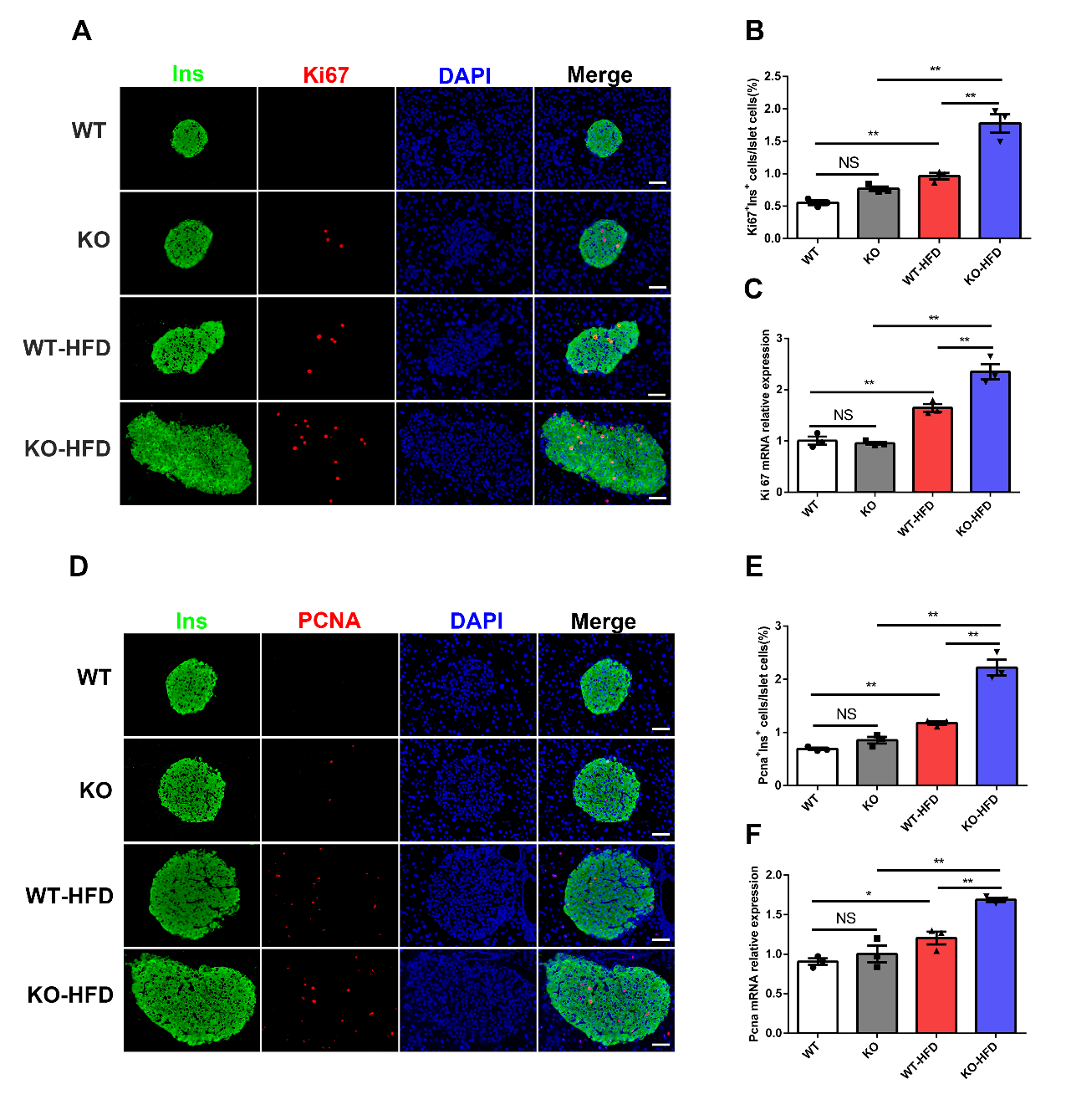
圖2
細胞增殖過程最終需要通過加速細胞周期的運轉而得以實現�,而細胞周期受到各種細胞周期蛋白、細胞周期蛋白依賴激酶及細胞周期相關的抑制因子等的調節(jié)�����。細胞周期蛋白(Cyclins)和細胞周期蛋白依賴激酶(Cdks)組成復合物,促進各時期細胞周期的時相轉換�。課題組進一步采用Western blot和RT-qPCR檢測了細胞周期調節(jié)因子的變化,結果表明����,TNXIP基因敲除能夠促進高脂喂養(yǎng)誘導的肥胖模型小鼠胰島β細胞細胞增殖周期進程(圖3)�。
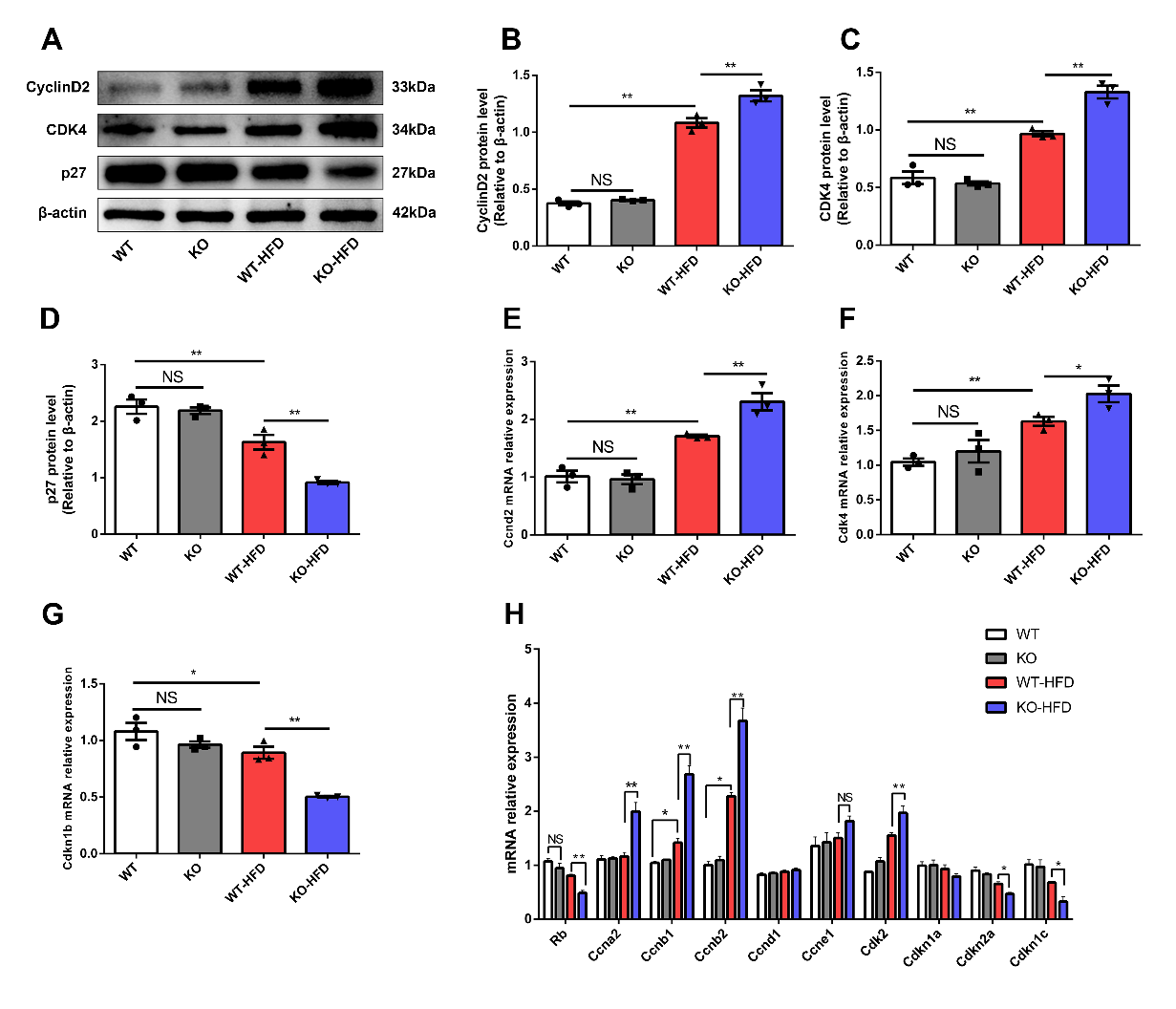
圖3
來自于細胞外的促增殖激素或生長因子包括血小板源性生長因子、胰島素����、葡萄糖、生長激素和胰高血糖素樣肽-1(GLP-1)等通過相應受體�,激活多種細胞內信號轉導途徑參與胰島β細胞增殖的調控,其中PI3K/AKT���、ERK��、Wnt/β-catenin是最主要的增殖調控信號通路�。為了進一步闡明TXNIP對胰島β細胞增殖的調控機制����,該課題組檢測了參與胰島β細胞增殖調控的信號通路,結果發(fā)現TXNIP基因敲除在高脂喂養(yǎng)的小鼠中能夠激活PI3K/AKT信號通路(圖4)�。
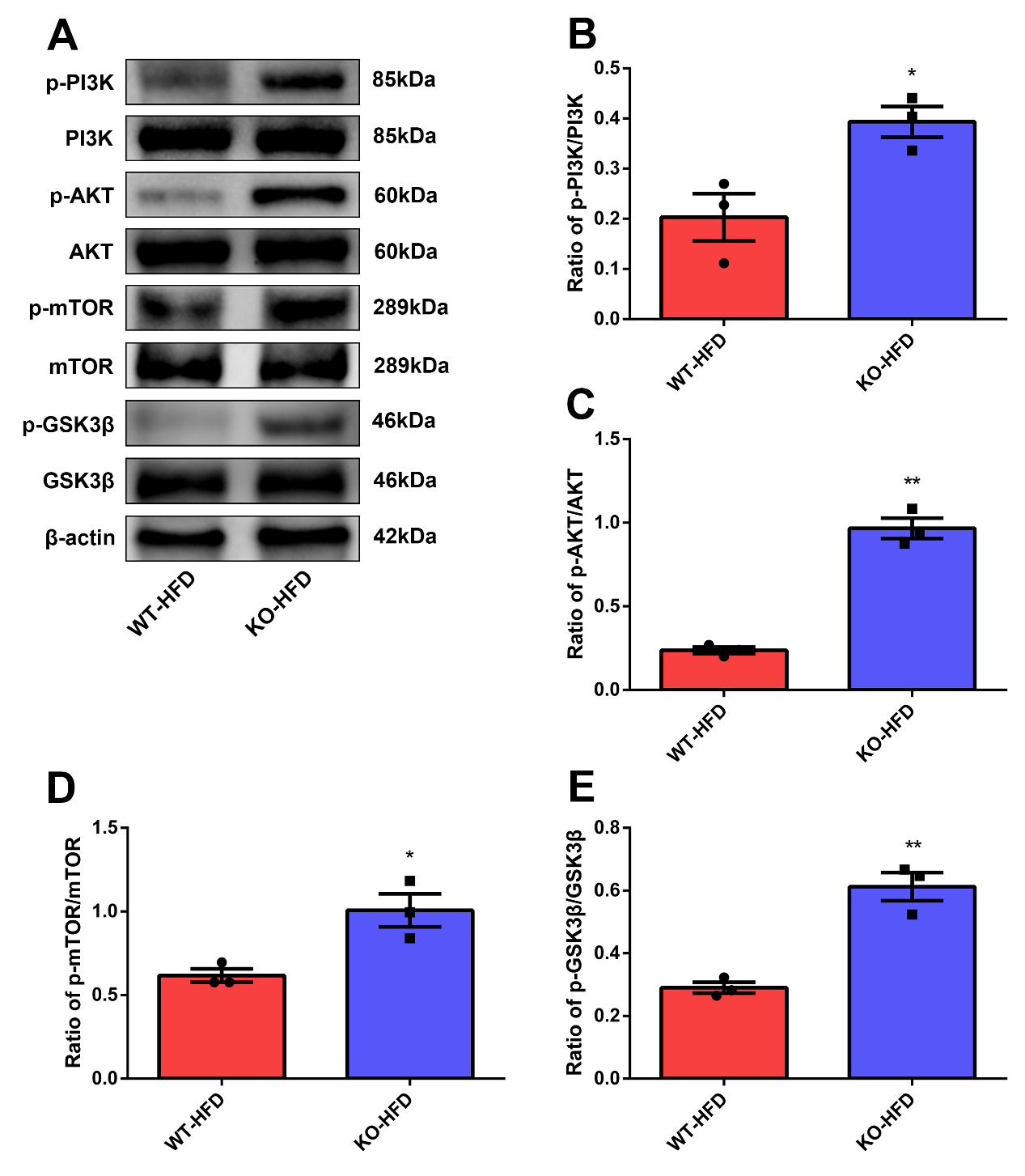
圖4
綜上所述,TXNIP基因敲除在高脂喂養(yǎng)誘導的肥胖模型小鼠中能夠促進胰島β細胞的代償性增殖,并通過激活PI3K/AKT信號通路參與胰島β細胞的增殖調控�����。
該研究結果已在Endocr Connect上發(fā)表����。論文第一署名單位為山西醫(yī)科大學。山西醫(yī)科大學基礎醫(yī)學院2018級博士研究生雷占東為論文的第一作者�。通訊作者為博士生導師焦向英教授。該研究得到山西省自然科學基金的資助�。