第二臨床醫(yī)學(xué)院神經(jīng)內(nèi)科薛國芳課題組首次觀察到新型GLP-1/GIP雙受體激動劑DA3-CH具有抑制癲癇發(fā)生的神經(jīng)保護作用

圖1
薛國芳課題組首次觀察到新型GLP-1/GIP雙受體激動劑DA3-CH具有抑制癲癇發(fā)生的神經(jīng)保護作用��,研究成果“The novel GLP-1/GIP dual receptor agonist DA3-CH is neuroprotective in the pilocarpine-induced epileptogenesis rat model”于2019年5月7日收錄于《Epilepsy Research》(圖1)�。
癲癇是最常見的神經(jīng)系統(tǒng)疾病之一�,影響全球高達1%的人口�����。發(fā)達國家的終身癲癇發(fā)病率中位數(shù)為5.8‰��,發(fā)展中國家為10.3‰��。癲癇由多種多樣的病因引起,表現(xiàn)為大腦神經(jīng)元超興奮性和超同步性異常放電��,以自發(fā)性復(fù)發(fā)性癲癇發(fā)作(recurrent spontaneous seizures, SRS)為特征��。癲癇持續(xù)狀態(tài)(status epilepticus , SE)是癲癇發(fā)作最嚴重的形式���,易誘發(fā)癲癇發(fā)生,進展為慢性癲癇���,出現(xiàn)SRS����。癲癇發(fā)作指一簇神經(jīng)元過度放電激發(fā)的一次短暫臨床發(fā)作���,而癲癇發(fā)生指致癇灶形成和成熟的慢性過程��。目前可獲得的臨床一線抗癲癇藥物(antiepileptic drugs, AEDs)對近三分之一的癲癇患者無效或產(chǎn)生不可耐受的副作用�����,其主要干預(yù)神經(jīng)元功能,調(diào)控突觸興奮和突觸抑制��,僅可控制癲癇發(fā)作�����,并不能阻止癲癇發(fā)生。因此�,抑制癲癇發(fā)生可能是一種潛在的新型治療策略。
癲癇發(fā)生被定義為大腦由正常生理狀態(tài)轉(zhuǎn)變?yōu)橹掳B狀態(tài)的慢性動態(tài)演變過程����,其可由多種初始事件或危險因素誘發(fā),例如癲癇持續(xù)狀態(tài)�����、創(chuàng)傷性腦損傷��、腦卒中��、感染和化學(xué)神經(jīng)中毒等����,經(jīng)過復(fù)雜多樣的病理生理學(xué)變化�,最終導(dǎo)致局部神經(jīng)元結(jié)構(gòu)和功能紊亂,致癇灶逐漸成熟��,形成慢性癲癇��。傳統(tǒng)AEDs 的分子靶點為抑制神經(jīng)元的異常放電及擴散�����,并不能阻止神經(jīng)元破壞的病理過程��,而后者是導(dǎo)致 SRS 的原因�?;趧游锛叭祟惏d癇的研究,癲癇發(fā)生的病理生理學(xué)動態(tài)變化包括離子通道激活�、炎癥和神經(jīng)膠質(zhì)反應(yīng)���、興奮毒性細胞凋亡��、血腦屏障破壞、表觀遺傳失調(diào)�、神經(jīng)變性和軸突生芽、苔蘚纖維發(fā)芽�、原纖維性神經(jīng)膠質(zhì)增生����、海馬硬化等。其中����,神經(jīng)炎癥反應(yīng)和細胞凋亡屬癲癇發(fā)生的始動因素,且參與癲癇發(fā)生的整個過程����,在癲癇發(fā)生中具有關(guān)鍵作用。
胰高血糖素樣肽-1(glucagon-like peptide-1, GLP-1)和葡萄糖依賴性促胰島素樣肽(glucose-dependent insulinotropic polypeptide, GIP)均屬腸促胰島素����,可促進胰島素分泌,抑制胰高血糖素分泌�����,其類似物已用于2型糖尿病的治療��,且其降糖作用呈葡萄糖依賴性�。近年的研究發(fā)現(xiàn)�,GLP-1和GIP還具有神經(jīng)保護作用����,在卒中�����、阿爾茨海默病(Alzheimer's disease, AD)��、帕金森?���。?a href="link:Parkinson%27s" style="text-decoration: none;">Parkinson's disease, PD)等神經(jīng)系統(tǒng)疾病動物模型中可通過抑制神經(jīng)膠質(zhì)細胞激活和促炎因子釋放���、抑制氧化應(yīng)激和細胞凋亡等方面發(fā)揮神經(jīng)保護作用���,且GLP-1/GIP雙受體激動劑的作用優(yōu)于選擇性單受體激動劑���。
研究采用經(jīng)典的匹羅卡品SE模型誘發(fā)癲癇發(fā)生����,給予新型GLP-1/GIP雙受體激動劑DA3-CH進行干預(yù)��,通過免疫組織化學(xué)和蛋白印跡分析方法檢測SE后12h�����、1d、3d���、7d大鼠尾靜脈空腹血糖水平以及海馬中星形膠質(zhì)細胞激活標(biāo)志物膠質(zhì)纖維酸性蛋白(glial fibrillary acidic protein, GFAP)����、小膠質(zhì)細胞激活標(biāo)志物離子鈣接頭分子-1(ionized calcium-binding adaptor molecule-1, Iba-1)、促炎因子白細胞介素-1β(interleukin-1β, IL-β)和腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)���、凋亡相關(guān)蛋白Bax和Bcl-2�、神經(jīng)元核抗原NeuN(neuronal nuclei)的表達水平����,評估DA3-CH對大鼠SE后神經(jīng)炎癥反應(yīng)�、細胞凋亡和神經(jīng)元丟失的影響。研究結(jié)果表明��,DA3-CH干預(yù)對非糖尿病大鼠血糖水平無影響(圖2),且可抑制SE后GFAP�、Iba-1、IL-1β��、TNF-α、Bax的表達����,同時促進SE后Bcl-2、NeuN的表達(圖3-6)�����。研究結(jié)果表明����,新型GLP-1/GIP 雙受體激動劑 DA3-CH 可抑制匹羅卡品誘導(dǎo)的大鼠SE后神經(jīng)炎癥反應(yīng)���、細胞凋亡和神經(jīng)元丟失�,具有抑制癲癇發(fā)生的潛在神經(jīng)保護作用,可能為探索抑制癲癇發(fā)生的新型治療策略提供實驗基礎(chǔ)�����。
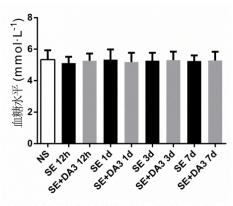
圖2各組大鼠空腹尾靜脈血糖水平
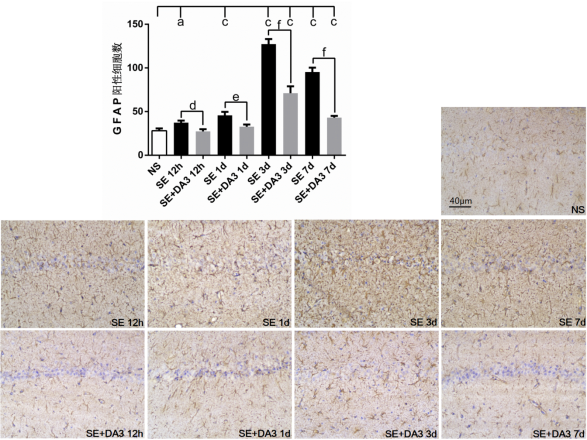
圖3各組大鼠海馬CA1區(qū)GFAP陽性細胞數(shù)及免疫組織化學(xué)圖片(×200)
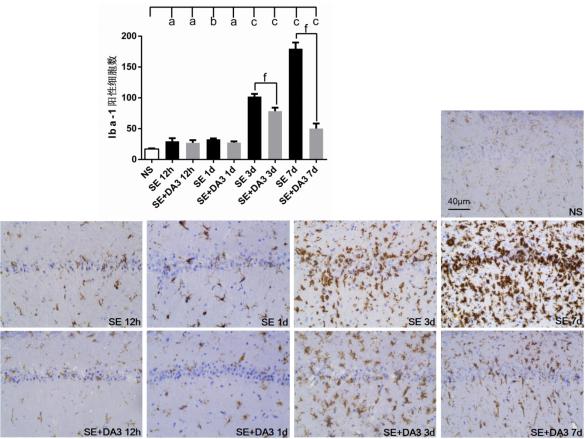
圖4各組大鼠海馬CA1區(qū)Iba-1陽性細胞數(shù)及免疫組織化學(xué)圖片(×200)
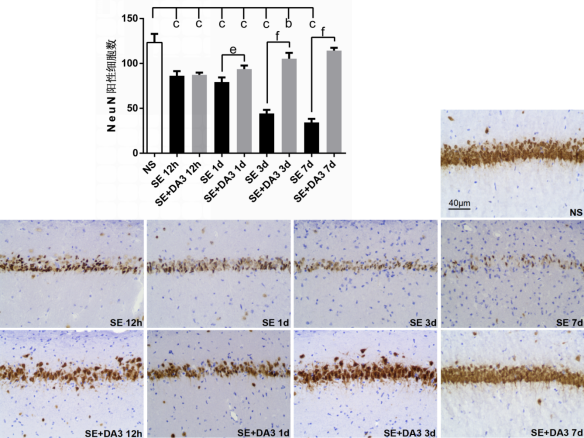
圖5各組大鼠海馬CA1區(qū)NeuN陽性細胞數(shù)及免疫組織化學(xué)圖片(×200)
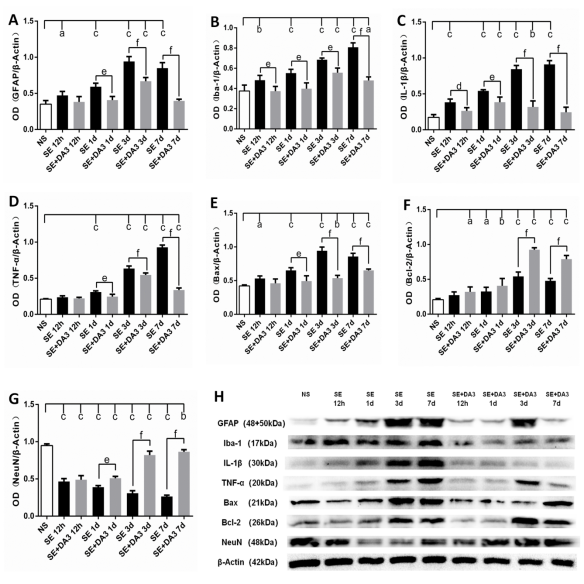
圖6各組大鼠海馬組織GFAP、Iba-1����、IL-1β���、TNF-α、Bax����、Bcl-2和NeuN相對OD值及western blot蛋白條帶
薛國芳副主任醫(yī)師為通信作者,田淼晶碩士為第一作者�����,王瑞芳碩士����、Christian H?lscher教授��、米茹麟碩士��、袁振宇碩士及李東芳主任醫(yī)師為共同作者。本課題承蒙國家自然科學(xué)基金和中國抗癲癇協(xié)會癲癇科研基金-UCB基金等資助�。